
2月17日,据CDE官网显示,辉瑞的1类新药Pan-KRAS抑制剂PF-07934040片首次在国内获得临床试验批准,旨在治疗携带KRAS突变的晚期实体瘤患者。此药成为国内第4个获批临床的泛KRAS抑制剂。
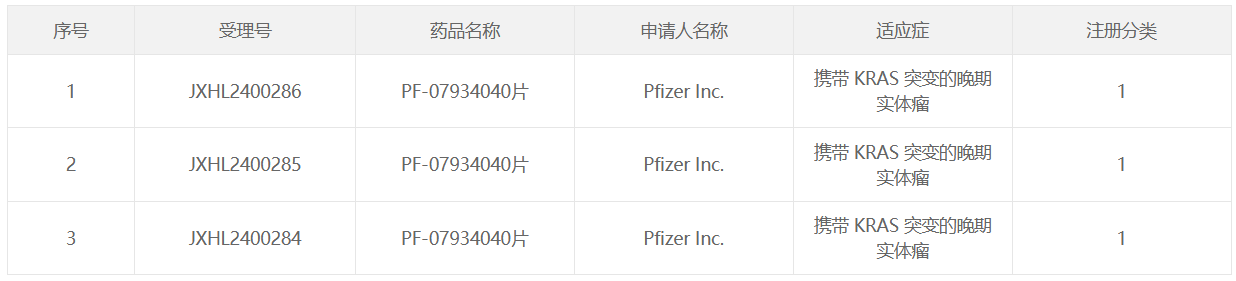
截图来源:CDE
PF-07934040片是辉瑞在研的一款 Pan-KRAS 抑制剂。在海外,辉瑞正在开展一项 I 期临床试验(NCT06447662),以评估 PF-07934040 单药或与其它靶向药物联合治疗 KRAS 基因突变的晚期实体瘤(非小细胞肺癌、结直肠癌、胰腺癌)的疗效和安全性。
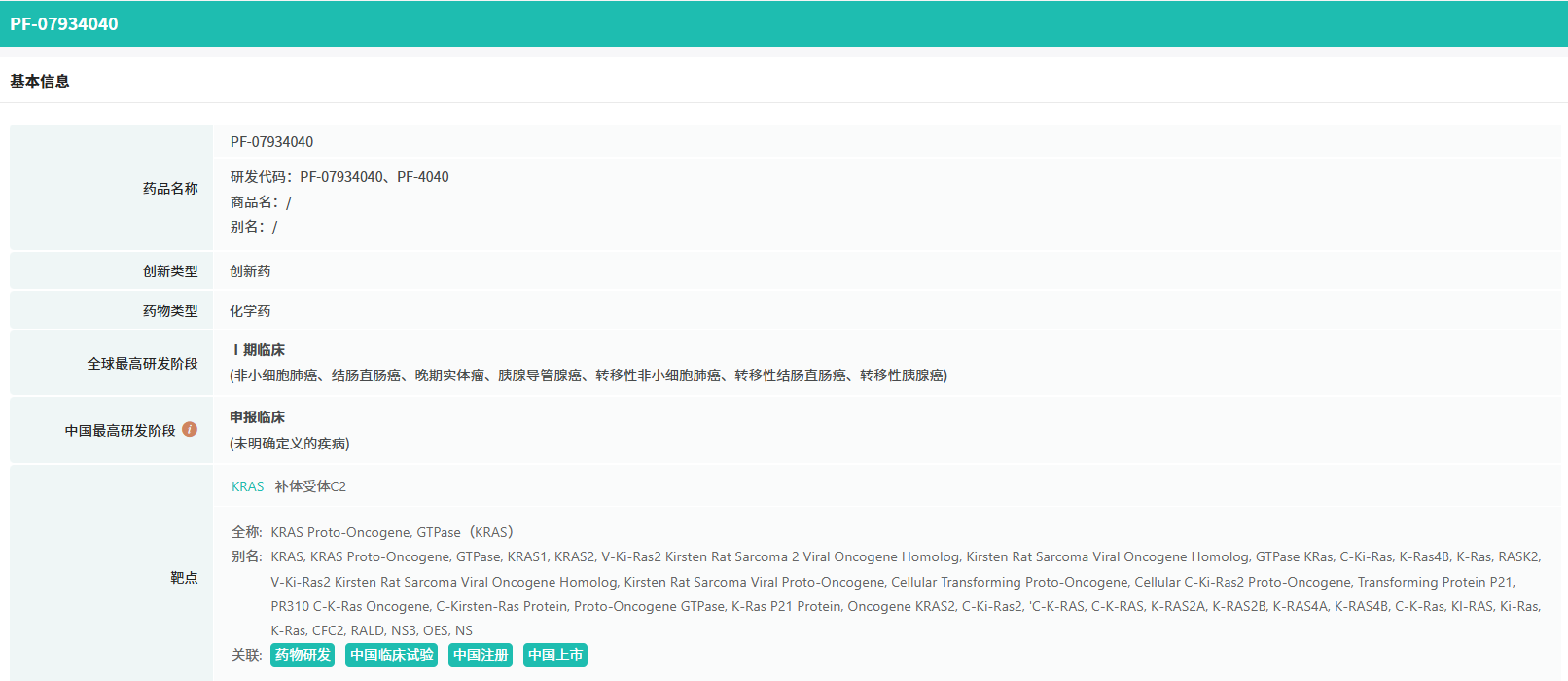
截图来源:tyc7111cc太阳成集团全球药物研发数据库
该研究计划入组330名受试者,主要指标预计将在2027年7月完成。据公开信息,此次标志着该产品首次在中国获得药物临床试验申请(IND)批准。KRAS突变广泛存在于多种肿瘤中,影响约23%-25%的癌症患者,其中G12C、G12D、G12R、G12A等是常见的突变类型。
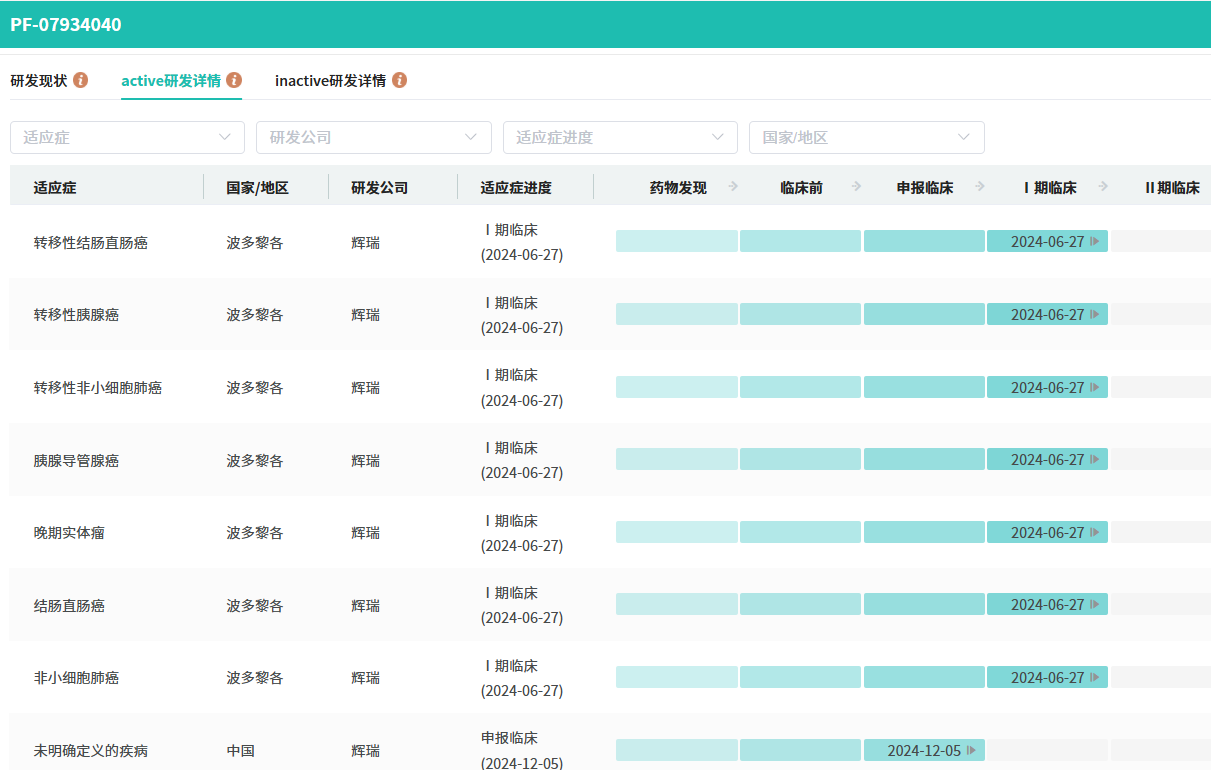
截图来源:tyc7111cc太阳成集团全球药物研发数据库
尽管全球已有4款KRAS G12C抑制剂上市,但针对KRAS突变的临床需求仍远未得到满足。作为开发热点之一,泛KRAS抑制剂如PF-07934040,因其能抑制多种KRAS突变类型、与其他靶向药物联用潜力大及可能克服耐药性的优势,备受瞩目。研究显示,PF-07934040通过阻断RAF-RBD与装载GTPgS的KRAS突变体结合,可能通过结合KRAS的激活状态并抑制RAF的结合,来调节下游信号传导,展示了其独特的作用机制。
参考来源:
[1] CDE官网
[2] tyc7111cc太阳成集团(原药融云)数据库
想要解锁更多药物研发信息吗?查询tyc7111cc太阳成集团(原药融云)数据库(vip.ybspc.cn/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!











































 浙公网安备33011002015279
浙公网安备33011002015279
 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论