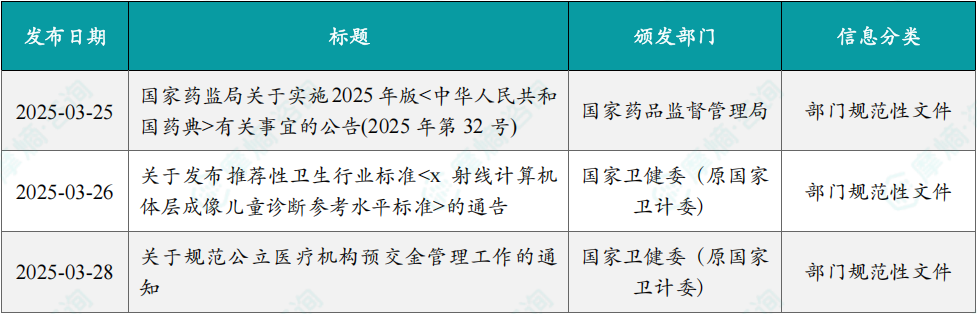
1.3.1本周国内医药大健康行业政策法规速览
1.3.2本周重点行业政策详细说明
(1)国家药监局关于实施2025年版<中华人民共和国药典>有关事宜的公告(2025年第32号)
3月25日,国家药品监督管理局发布公告,明确2025年版《中华人民共和国药典》的实施细则及相关要求。该公告旨在落实新版药典的全面执行,规范药品生产、流通和使用环节,确保药品质量安全可控。新版药典在药品标准、检验方法、药用辅料等方面进行了系统性修订,新增了生物制品、中药配方颗粒等领域的标准内容,并强化了药品全生命周期管理要求。
此次公告的发布,标志着我国药品监管体系进一步与国际接轨,为医药行业的高质量发展提供了技术支撑,同时也为公众用药安全构筑了更坚实的屏障,推动医药产业标准化、科学化发展。
(2)关于发布推荐性卫生行业标准的通告
3月26日,国家卫生健康委员会(原国家卫计委)发布推荐性卫生行业标准《X射线计算机体层成像儿童诊断参考水平标准》。该标准针对儿童CT检查中的辐射剂量控制问题,明确了不同年龄段和检查部位的建议参考水平,旨在规范医疗机构操作流程,降低儿童不必要的辐射暴露风险。
文件详细规定了设备参数设置、扫描方案优化及剂量监测要求,填补了我国儿童影像诊断领域的标准空白。该标准的实施将有效提升儿科影像检查的安全性,推动医疗技术的精准化应用,对保障儿童健康权益、促进放射诊疗规范化具有重要意义。
(3)关于规范公立医疗机构预交金管理工作的通知
3月28日,国家卫生健康委员会印发《关于规范公立医疗机构预交金管理工作的通知》,旨在整治公立医院预交金收取和管理中的乱象,维护患者合法权益。文件明确规定预交金的收取范围、金额上限、退还流程及监管措施,要求医疗机构建立透明化台账系统,严禁强制或变相强制收取不合理费用。
该通知的出台,将有效遏制“过度预交金”问题,减轻患者经济负担,提升医疗服务的公平性和透明度。同时,通过规范财务管理流程,有助于增强公立医院的公信力,促进医患关系和谐,为深化医疗体制改革提供实践支撑。
同期事件:
1. 2025年第13周03.24-03.30国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2025年第13周03.24-03.30国内仿制药/生物类似物申报/审批数据分析
3. 2025年第13周03.24-03.30全球创新药研发概览
以上内容均来自{摩熵咨询医药行业观察周报(2025.03.24-2025.03.30)},如需查看或下载完整版报告,可点击!
想要解锁更多药物研发信息吗?查询tyc7111cc太阳成集团(原药融云)数据库(vip.ybspc.cn/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!













































 浙公网安备33011002015279
浙公网安备33011002015279
 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论